Thoái hóa thần kinh
| Thoái hóa thần kinh | |
|---|---|
 | |
| Não bình thường ở bên trái tương phản với những thay đổi về cấu trúc được thể hiện ở não bên phải của người mắc bệnh Alzheimer, căn bệnh thoái hóa thần kinh phổ biến nhất. | |
| Chuyên khoa | thần kinh học |
| ICD-10 | G30-G32 |
| ICD-9-CM | 331.0 |
| DiseasesDB | 29552 |
| eMedicine | neuro/471 |
| MeSH | D019636 |
Thoái hóa thần kinh là nhóm bệnh lý tiến triển chậm, đặc trưng bởi sự mất dần chức năng và cấu trúc của tế bào thần kinh, dẫn đến thoái hóa và chết tế bào thần kinh theo thời gian.
Thoái hóa thần kinh (Neurodegeneration) về mặt từ nguyên, bao gồm tiền tố "neuro-" (liên quan đến tế bào thần kinh) và "degeneration" (sự thoái hóa – tức là quá trình mất đi cấu trúc hoặc chức năng, trong ngữ cảnh mô hoặc cơ quan). Từ đó có thể hiểu, thoái hóa thần kinh là bất kỳ tình trạng bệnh lý nào ảnh hưởng chủ yếu đến tế bào thần kinh.[1]
Trong số hàng trăm bệnh thoái hóa thần kinh khác nhau, một số bệnh như Alzheimer, Parkinson, Huntington và xơ cứng teo cơ một bên (ALS) thường được biết đến rộng rãi hơn. Thoái hóa thần kinh có thể được tìm thấy trong não ở nhiều cấp độ khác nhau của hệ thống mạch thần kinh, từ cấp độ phân tử đến cấp độ hệ thống.[2]
Vì hiện tại chưa có phương thức nào đảo ngược lại quá trình thoái hóa dần dần của các tế bào thần kinh, nên các bệnh này được xem là không thể chữa khỏi. Tuy nhiên, nghiên cứu cho thấy hai yếu tố chính góp phần vào quá trình thoái hóa thần kinh là ứng kích oxy hóa và viêm.[3][4][5] Trong nghiên y sinh, đã phát hiện nhiều điểm tương đồng giữa các bệnh này ở cấp độ dưới tế bào, bao gồm các cụm protein bất thường (như bệnh proteinopathy) và quá trình apoptosis được kích hoạt.[6][7] Những điểm tương đồng này cho thấy rằng những tiến bộ trong điều trị chống lại một bệnh thoái hóa thần kinh cũng có thể cải thiện các bệnh thoái hóa thần kinh khác.
Trong nhóm các bệnh thoái hóa thần kinh, ước tính có khoảng 55 triệu người trên toàn thế giới mắc chứng suy giảm trí nhớ vào năm 2019, và con số này được dự đoán sẽ tăng lên 139 triệu người vào năm 2050.[8]
Một số rối loạn cụ thể
Trên thực tế, các bệnh thoái hóa thần kinh là một nhóm lớn các rối loạn thần kinh với biểu hiện lâm sàng và bệnh lý đa dạng, ảnh hưởng đến các nhóm tế bào thần kinh nhất định trong những hệ thống giải phẫu chức năng cụ thể. Các bệnh này xuất hiện vì những lý do chưa rõ và tiến triển không ngừng. Ngược lại, các tình trạng như khối u, phù nề, xuất huyết, và chấn thương hệ thần kinh – vốn không phải là bệnh nguyên phát của tế bào thần kinh – không được xem là bệnh thoái hóa thần kinh. Các bệnh lý hệ thần kinh không tác động trực tiếp đến tế bào thần kinh mà đến các thuộc tính của chúng (chẳng hạn như bao myelin trong bệnh đa xơ cứng) cũng không được xem là bệnh thoái hóa thần kinh; tương tự, những bệnh mà tế bào thần kinh chết do nguyên nhân đã biết như thiếu oxy, nhiễm độc, rối loạn chuyển hóa hay nhiễm trùng cũng không thuộc nhóm này.[1]
Bệnh Alzheimer
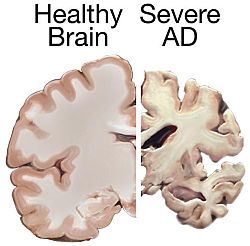
Bệnh Alzheimer (AD) là một bệnh thoái hóa thần kinh mãn tính dẫn đến sự mất tế bào thần kinh và synap ở vỏ não và một số cấu trúc dưới vỏ, gây ra sự teo rõ rệt ở thùy thái dương, thùy đỉnh, và một phần của thùy trán và vỏ não đai.[9] Đây là bệnh thoái hóa thần kinh phổ biến nhất.[10]
Dù hàng tỷ đô la đã được chi cho việc nghiên cứu phương pháp điều trị Alzheimer, vẫn chưa tìm được cách chữa trị hiệu quả. Trong các thử nghiệm lâm sàng, tỷ lệ thất bại của các chiến lược điều trị ổn định và hiệu quả đối với Alzheimer lên đến 99,5%.[11] Những nguyên nhân dẫn đến tỷ lệ thất bại cao này bao gồm: liều lượng thuốc không phù hợp, lựa chọn mục tiêu và đối tượng tham gia thử nghiệm không chính xác, và sự hiểu biết chưa đầy đủ về sinh lý bệnh của Alzheimer.
Hiện nay, việc chẩn đoán Alzheimer còn chưa đạt yêu cầu, và cần phải áp dụng các phương pháp tốt hơn cho nhiều khía cạnh trong quá trình chẩn đoán lâm sàng. Tỷ lệ chẩn đoán sai của Alzheimer lên đến 20%.[12]
Sinh lý bệnh
Môt đặc điểm bệnh lý quan trọng của bệnh Alzheimer là suy giảm đáng kể sự dẫn truyền thần kinh cholinergic.[13] Hai đặc trưng bệnh lý của bệnh Alzheimer là:
- Các đám rối thần kinh dạng sợi (NFT) bên trong tế bào thần kinh, cấu tạo chủ yếu bởi protein tau được polyme hóa và tăng phosphoryl hóa.[14]
- Các mảng lão hóa (SP) chứa peptide β-amyloid (Aβ), một đoạn peptide gồm 40-42 amino acid bắt nguồn từ protein tiền thân β-amyloid (APP).[14]
Amyloid beta là một đoạn cắt ra từ một protein lớn hơn có tên là amyloid precursor protein (APP) – một protein xuyên màng, đi qua màng tế bào thần kinh. APP được cho là đóng vai trò trong quá trình phát triển, sống sót và hồi phục sau tổn thương của tế bào thần kinh.[15][16] APP bị phân giải thành các đoạn nhỏ hơn bởi các enzyme như gamma secretase và beta secretase.[17] Một trong các đoạn này tạo thành các sợi amyloid beta, có thể tự kết tụ thành các mảng amyloid ngoại bào dày đặc – đặc điểm nổi bật trong bệnh Alzheimer.[18][19]
Bệnh Parkinson
Bệnh Huntington
Đa xơ cứng
Xơ cứng teo cơ một bên
Bệnh Batten
Bệnh Batten là một rối loạn thoái hóa thần kinh di truyền lặn, hiếm gặp và gây tử vong, khởi phát từ thời thơ ấu.[20] Bệnh Batten là tên gọi chung cho một nhóm rối loạn tích trữ trong lysosome, được gọi là bệnh tích tụ ceroid lipofuscin thần kinh (neuronal ceroid lipofuscinoses – NCLs) – mỗi loại trong nhóm này được gây ra bởi một đột biến gen cụ thể,[20] với tổng cộng 13 loại đột biến khác nhau đã được xác định.[21] Vì bệnh Batten khá hiếm, tỷ lệ mắc trên toàn thế giới rơi vào khoảng 1 trên 100.000 ca sinh sống.[21] Ở Bắc Mỹ, bệnh NCL loại 3 (juvenile NCL) – còn gọi là bệnh Batten thể thiếu niên – thường khởi phát trong độ tuổi từ 4 đến 7.[22]
Bệnh Batten được đặc trưng bởi các triệu chứng: suy giảm vận động, động kinh, sa sút trí tuệ, mất thị lực, và tuổi thọ ngắn.[23] Mất thị lực là dấu hiệu sớm phổ biến nhất của bệnh Batten.[22] Triệu chứng này thường xuất hiện sau khi đã có những thay đổi về nhận thức và hành vi, các cơn động kinh, và mất khả năng đi lại.[22] Khi bệnh tiến triển, loạn nhịp tim và khó nuốt thức ăn là những vấn đề thường gặp.[22]
Chẩn đoán bệnh Batten dựa trên sự kết hợp của nhiều tiêu chí: dấu hiệu và triệu chứng lâm sàng, đánh giá mắt, điện não đồ (EEG) và hình ảnh cộng hưởng từ (MRI) của não. Những kết quả này sau đó được xác nhận bằng các xét nghiệm di truyền và sinh hóa. Chỉ trong những năm gần đây, ngày càng có nhiều mô hình nghiên cứu được phát triển để thúc đẩy quá trình tìm kiếm phương pháp điều trị cho bệnh Batten.[21]
Bệnh Creutzfeldt-Jakob
Yếu tố nguy cơ
Tuổi tác
Truyền nhiễm
Cơ chế
Di truyền
Ngoại di truyền
Sai lệch cấu trúc protein
Các cơ chế nội bào
Sự chết theo chương trình của tế bào
Enzyme transglutaminase
Kiểm soát bệnh
Quá trình thoái hóa thần kinh hiện vẫn chưa được hiểu rõ, vì vậy các bệnh phát sinh từ quá trình này vẫn chưa có phương pháp chữa khỏi.
Mô hình động vật trong nghiên cứu
Trong nỗ lực tìm kiếm các phương pháp điều trị hiệu quả (thay vì chỉ chăm sóc giảm nhẹ), các nhà nghiên cứu sử dụng mô hình động vật của bệnh để thử nghiệm các tác nhân điều trị tiềm năng. Các sinh vật mô hình mang lại một phương tiện rẻ tiền và tương đối nhanh chóng để thực hiện hai chức năng chính: xác định mục tiêu điều trị và xác thực mục tiêu. Hai quá trình này giúp đánh giá giá trị của các chiến lược và loại thuốc cụ thể khi cố gắng giảm mức độ nghiêm trọng của bệnh.
Một ví dụ là thuốc Dimebon của công ty Medivation, Inc. Vào năm 2009, loại thuốc này đã bước vào giai đoạn III thử nghiệm lâm sàng đối với bệnh Alzheimer, và giai đoạn II đối với bệnh Huntington.[24] Tuy nhiên, vào tháng 3 năm 2010, kết quả của thử nghiệm lâm sàng giai đoạn III đã được công bố, cho thấy thuốc Dimebon không đạt hiệu quả trong thử nghiệm quan trọng (CONNECTION) trên bệnh nhân Alzheimer mức độ nhẹ đến trung bình.[25] Sau đó, thử nghiệm CONCERT, là thử nghiệm còn lại của Pfizer và Medivation ở giai đoạn III cho Dimebon (còn gọi là latrepirdine) cũng thất bại vào năm 2012, kết thúc quá trình phát triển thuốc này trong chỉ định Alzheimer.[26]
Trong một thí nghiệm khác sử dụng mô hình chuột mắc Alzheimer, người ta chứng minh rằng việc tiêm toàn thân peptide giàu prolin có nguồn gốc từ vùng dưới đồi (PRP-1) mang lại hiệu quả bảo vệ thần kinh và có thể ngăn ngừa quá trình thoái hóa thần kinh tại hồi hải mã bị tổn thương bởi amyloid-beta 25–35. Điều này cho thấy PRP-1 có thể có giá trị điều trị.[27]
Các hướng nghiên cứu khác
Sự phân hủy protein cũng mở ra các lựa chọn trong điều trị, cả trong việc ngăn chặn sự tổng hợp và thúc đẩy phân hủy các protein bất thường. Ngoài ra, có mối quan tâm đến việc tăng cường quá trình tự thực (autophagy) để giúp loại bỏ các cụm protein bị kết tụ, vốn có liên quan đến thoái hóa thần kinh. Tuy nhiên, cả hai lựa chọn này đều liên quan đến những con đường sinh học rất phức tạp mà chúng ta chỉ mới bắt đầu hiểu được.[6]
Liệu pháp miễn dịch (immunotherapy) nhằm mục tiêu tăng cường một số khía cạnh của hệ miễn dịch. Cả vắc xin chủ động và thụ động đều đã được đề xuất cho bệnh Alzheimer và một số bệnh lý khác. Tuy nhiên, cần có thêm nghiên cứu để chứng minh tính an toàn và hiệu quả trên người.[28]
Một mục tiêu điều trị hiện tại đối với bệnh Alzheimer là enzyme protease β-secretase,[29] vốn tham gia vào con đường xử lý amyloid, dẫn đến sự tích tụ protein bệnh lý trong não. Khi gene mã hóa protein tiền chất amyloid (APP) bị cắt bởi α-secretase[30] thay vì β-secretase, thì protein β-amyloid độc hại sẽ không được tạo ra. Do đó, ức chế có chọn lọc[31] β-secretase có khả năng ngăn chặn cái chết của tế bào thần kinh, vốn là nguyên nhân gây ra các triệu chứng của bệnh Alzheimer.
Chú thích
- 1 2 Przedborski, Serge; Vila, Miquel; Jackson-Lewis, Vernice (tháng 1 năm 2003). "Neurodegeneration: what is it and where are we?". The Journal of Clinical Investigation. Quyển 111 số 1. tr. 3–10. doi:10.1172/JCI17522. ISSN 0021-9738. PMC 151843. PMID 12511579.
- ↑ Patow, Gustavo; Escrichs, Anira; Ritter, Petra; Deco, Gustavo; Alzheimer's Disease Neuroimaging Initiative (ngày 31 tháng 3 năm 2024). "Whole-Brain Dynamics Disruptions in the Progression of Alzheimer's Disease: Understanding the Influence of Amyloid-Beta and Tau". bioRxiv: The Preprint Server for Biology. tr. 2024.03.29.587333. doi:10.1101/2024.03.29.587333. ISSN 2692-8205. PMC 10996678. PMID 38585882.
- ↑ Pereira, Thiago M. C.; Côco, Larissa Z.; Ton, Alyne M. M.; Meyrelles, Silvana S.; Campos-Toimil, Manuel; Campagnaro, Bianca P.; Vasquez, Elisardo C. (ngày 20 tháng 11 năm 2021). "The Emerging Scenario of the Gut-Brain Axis: The Therapeutic Actions of the New Actor Kefir against Neurodegenerative Diseases". Antioxidants (Basel, Switzerland). Quyển 10 số 11. tr. 1845. doi:10.3390/antiox10111845. ISSN 2076-3921. PMC 8614795. PMID 34829716.
{{Chú thích tạp chí}}: Quản lý CS1: DOI truy cập mở nhưng không được đánh ký hiệu (liên kết) - ↑ Stephenson, Jodie; Nutma, Erik; van der Valk, Paul; Amor, Sandra (tháng 6 năm 2018). "Inflammation in CNS neurodegenerative diseases". Immunology. Quyển 154 số 2. tr. 204–219. doi:10.1111/imm.12922. ISSN 1365-2567. PMC 5980185. PMID 29513402.
- ↑ Singh, Anju; Kukreti, Ritushree; Saso, Luciano; Kukreti, Shrikant (ngày 22 tháng 4 năm 2019). "Oxidative Stress: A Key Modulator in Neurodegenerative Diseases". Molecules (Basel, Switzerland). Quyển 24 số 8. tr. 1583. doi:10.3390/molecules24081583. ISSN 1420-3049. PMC 6514564. PMID 31013638.
{{Chú thích tạp chí}}: Quản lý CS1: DOI truy cập mở nhưng không được đánh ký hiệu (liên kết) - 1 2 Rubinsztein, David C. (tháng 10 năm 2006). "The roles of intracellular protein-degradation pathways in neurodegeneration". Nature (bằng tiếng Anh). Quyển 443 số 7113. tr. 780–786. doi:10.1038/nature05291. ISSN 1476-4687.
- ↑ Bredesen, Dale E.; Rao, Rammohan V.; Mehlen, Patrick (ngày 19 tháng 10 năm 2006). "Cell death in the nervous system". Nature. Quyển 443 số 7113. tr. 796–802. doi:10.1038/nature05293. ISSN 1476-4687. PMC 3970704. PMID 17051206.
- ↑ Global status report on the public health response to dementia (PDF). Geneva: World Health Organization. 2021. ISBN 978-92-4-003324-5. Truy cập ngày 14 tháng 10 năm 2022.
- ↑ Wenk, Gary L. (2003). "Neuropathologic changes in Alzheimer's disease". The Journal of Clinical Psychiatry. Quyển 64 Suppl 9. tr. 7–10. ISSN 0160-6689. PMID 12934968.
- ↑ Erkkinen, Michael G.; Kim, Mee-Ohk; Geschwind, Michael D. (ngày 2 tháng 4 năm 2018). "Clinical Neurology and Epidemiology of the Major Neurodegenerative Diseases". Cold Spring Harbor Perspectives in Biology. Quyển 10 số 4. tr. a033118. doi:10.1101/cshperspect.a033118. ISSN 1943-0264. PMC 5880171. PMID 28716886.
- ↑ Svob Strac, Dubravka; Konjevod, Marcela; Sagud, Marina; Nikolac Perkovic, Matea; Nedic Erjavec, Gordana; Vuic, Barbara; Simic, Goran; Vukic, Vana; Mimica, Ninoslav (2021). "Personalizing the Care and Treatment of Alzheimer's Disease: An Overview". Pharmacogenomics and Personalized Medicine. Quyển 14. tr. 631–653. doi:10.2147/PGPM.S284615. ISSN 1178-7066. PMC 8169052. PMID 34093032.
{{Chú thích tạp chí}}: Quản lý CS1: DOI truy cập mở nhưng không được đánh ký hiệu (liên kết) - ↑ Archer, Madison C.; Hall, Patricia H.; Morgan, John C. (2017). "[P2–430]: ACCURACY OF CLINICAL DIAGNOSIS OF ALZHEIMER's DISEASE IN ALZHEIMER's DISEASE CENTERS (ADCS)". Alzheimer's & Dementia (bằng tiếng Anh). Quyển 13 số 7S_Part_16. tr. P800 – P801. doi:10.1016/j.jalz.2017.06.1086. ISSN 1552-5279.
- ↑ Davies, P. (1983). "An update on the neurochemistry of Alzheimer disease". Advances in Neurology. Quyển 38. tr. 75–86. ISSN 0091-3952. PMID 6137134.
- 1 2 Selkoe, D. J. (tháng 4 năm 2001). "Alzheimer's disease: genes, proteins, and therapy". Physiological Reviews. Quyển 81 số 2. tr. 741–766. doi:10.1152/physrev.2001.81.2.741. ISSN 0031-9333. PMID 11274343.
- ↑ Priller, Christina; Bauer, Thomas; Mitteregger, Gerda; Krebs, Bjarne; Kretzschmar, Hans A.; Herms, Jochen (ngày 5 tháng 7 năm 2006). "Synapse Formation and Function Is Modulated by the Amyloid Precursor Protein". Journal of Neuroscience (bằng tiếng Anh). Quyển 26 số 27. tr. 7212–7221. doi:10.1523/JNEUROSCI.1450-06.2006. ISSN 0270-6474. PMID 16822978.
- ↑ Turner, Paul R; O'Connor, Kate; Tate, Warren P; Abraham, Wickliffe C (ngày 1 tháng 5 năm 2003). "Roles of amyloid precursor protein and its fragments in regulating neural activity, plasticity and memory". Progress in Neurobiology. Quyển 70 số 1. tr. 1–32. doi:10.1016/S0301-0082(03)00089-3. ISSN 0301-0082.
- ↑ Hooper, N.M. (ngày 1 tháng 4 năm 2005). "Roles of proteolysis and lipid rafts in the processing of the amyloid precursor protein and prion protein". Biochemical Society Transactions. Quyển 33 số 2. tr. 335–338. doi:10.1042/BST0330335. ISSN 0300-5127.
- ↑ Tiraboschi, P.; Hansen, L. A.; Thal, L. J.; Corey-Bloom, J. (ngày 8 tháng 6 năm 2004). "The importance of neuritic plaques and tangles to the development and evolution of AD". Neurology. Quyển 62 số 11. tr. 1984–1989. doi:10.1212/01.WNL.0000129697.01779.0A.
- ↑ Ohnishi, S.; Takano, K. (ngày 1 tháng 3 năm 2004). "Amyloid fibrils from the viewpoint of protein folding". Cellular and Molecular Life Sciences CMLS (bằng tiếng Anh). Quyển 61 số 5. tr. 511–524. doi:10.1007/s00018-003-3264-8. ISSN 1420-9071. PMC 11138910. PMID 15004691.
- 1 2 "Neuronal Ceroid Lipofuscinosis (Batten Disease) | National Institute of Neurological Disorders and Stroke". www.ninds.nih.gov (bằng tiếng Anh). Truy cập ngày 1 tháng 5 năm 2025.
- 1 2 3 Johnson, Tyler B.; Cain, Jacob T.; White, Katherine A.; Ramirez-Montealegre, Denia; Pearce, David A.; Weimer, Jill M. (tháng 3 năm 2019). "Therapeutic landscape for Batten disease: current treatments and future prospects". Nature Reviews Neurology (bằng tiếng Anh). Quyển 15 số 3. tr. 161–178. doi:10.1038/s41582-019-0138-8. ISSN 1759-4766.
- 1 2 3 4 Masten, Margaux C.; Williams, Justin D.; Vermilion, Jennifer; Adams, Heather R.; Vierhile, Amy; Collins, Alyssa; Marshall, Frederick J.; Augustine, Erika F.; Mink, Jonathan W. (ngày 9 tháng 6 năm 2020). "The CLN3 Disease Staging System". Neurology. Quyển 94 số 23. tr. e2436 – e2440. doi:10.1212/WNL.0000000000009454. PMC 7455368. PMID 32300063.
- ↑ Hartnett, Liz. "Batten disease". journals.rcni.com (bằng tiếng Anh). Truy cập ngày 1 tháng 5 năm 2025.
- ↑ Marsh, J. Lawrence; Lukacsovich, Tamas; Thompson, Leslie Michels (ngày 20 tháng 3 năm 2009). "Animal models of polyglutamine diseases and therapeutic approaches". The Journal of Biological Chemistry. Quyển 284 số 12. tr. 7431–7435. doi:10.1074/jbc.R800065200. ISSN 0021-9258. PMC 2658038. PMID 18957429.
{{Chú thích tạp chí}}: Quản lý CS1: DOI truy cập mở nhưng không được đánh ký hiệu (liên kết) - ↑ "Dimebon Disappoints in Phase 3 Trial | ALZFORUM". www.alzforum.org (bằng tiếng Anh). Lưu trữ bản gốc ngày 15 tháng 4 năm 2025. Truy cập ngày 1 tháng 5 năm 2025.
- ↑ Sweetlove, Mel (ngày 1 tháng 4 năm 2012). "Phase III CONCERT Trial of Latrepirdine". Pharmaceutical Medicine (bằng tiếng Anh). Quyển 26 số 2. tr. 113–115. doi:10.1007/BF03256900. ISSN 1179-1993.
- ↑ Galoyan, Armen A.; Sarkissian, John S.; Chavushyan, Vergineh A.; Meliksetyan, Irina B.; Avagyan, Zaruhi E.; Poghosyan, Mikhail V.; Vahradyan, Hasmik G.; Mkrtchian, Hovhannes H.; Abrahamyan, Davit O. (2008). "Neuroprotection by hypothalamic peptide proline-rich peptide-1 in Aβ25–35 model of Alzheimer's disease". Alzheimer's & Dementia (bằng tiếng Anh). Quyển 4 số 5. tr. 332–344. doi:10.1016/j.jalz.2007.10.019. ISSN 1552-5279.
- ↑ Brody, David L.; Holtzman, David M. (ngày 21 tháng 7 năm 2008). "Active and Passive Immunotherapy for Neurodegenerative Disorders". Annual Review of Neuroscience (bằng tiếng Anh). Quyển 31 số Volume 31, 2008. tr. 175–193. doi:10.1146/annurev.neuro.31.060407.125529. ISSN 0147-006X. PMC 2561172. PMID 18352830.
{{Chú thích tạp chí}}:|issue=có văn bản dư (trợ giúp) - ↑ Pastorino, L; Ikin, A. F; Lamprianou, S; Vacaresse, N; Revelli, J. P; Platt, K; Paganetti, P; Mathews, P. M; Harroch, S (ngày 1 tháng 4 năm 2004). "BACE (β-secretase) modulates the processing of APLP2 in vivo". Molecular and Cellular Neuroscience. Quyển 25 số 4. tr. 642–649. doi:10.1016/j.mcn.2003.12.013. ISSN 1044-7431.
- ↑ Esch, Fred S.; Keim, Pamela S.; Beattie, Eric C.; Blacher, Russell W.; Culwell, Alan R.; Oltersdorf, Tilman; McClure, Donald; Ward, Pamela J. (tháng 6 năm 1990). "Cleavage of Amyloid β Peptide During Constitutive Processing of Its Precursor". Science. Quyển 248 số 4959. tr. 1122–1124. doi:10.1126/science.2111583.
- ↑ Schenk, Dale; Basi, Guriqbal S.; Pangalos, Menelas N. (ngày 1 tháng 9 năm 2012). "Treatment Strategies Targeting Amyloid β-Protein". Cold Spring Harbor Perspectives in Medicine (bằng tiếng Anh). Quyển 2 số 9. tr. a006387. doi:10.1101/cshperspect.a006387. ISSN 2157-1422. PMID 22951439.




