Hội chứng nhược cơ Lambert–Eaton
| Hội chứng nhược cơ Lambert–Eaton | |
|---|---|
| Tên khác | Hội chứng Lambert–Eaton, hội chứng Eaton–Lambert, hội chứng nhược cơ, viêm cơ liên quan đến ung thư |
 | |
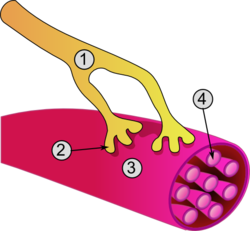
Khớp nối thần kinh cơ. Hội chứng nhược cơ Lambert–Eaton xuất hiện khi tự kháng thể tấn công vào màng trước synap. Bệnh nhược cơ Myasthenia gravis xuất hiện khi tự kháng thể tấn công vào thụ thể acetylcholin ở màng sau synap.
| |
| Khoa/Ngành | Thần kinh học |
| Dịch tễ | 3.4 người trên mỗi 1 triệu người[1] |
Hội chứng nhược cơ Lambert–Eaton (LEMS) là một rối loạn tự miễn hiếm gặp, đặc trưng bởi tình trạng yếu cơ ở các chi. Hội chứng này còn được gọi là hội chứng Lambert–Eaton, hội chứng Eaton–Lambert, và khi liên quan đến ung thư thì được gọi là bệnh cơ do ung thư.[2]
Khoảng 60% những người mắc hội chứng Lambert–Eaton có bệnh ác tính tiềm ẩn, phổ biến nhất là ung thư phổi tế bào nhỏ (SCLC), do đó hội chứng Lambert–Eaton được xem là một hội chứng cận u (tình trạng xảy ra do ung thư ở nơi khác trong cơ thể).[3] Cơ chế bệnh sinh là do các kháng thể tấn công vào các kênh calci đóng mở bằng điện áp ở màng trước synap, và có thể cả các protein khác ở đầu tận cùng dây thần kinh, trong khớp nối thần kinh cơ.[4] Chẩn đoán thường được xác nhận bằng điện cơ và xét nghiệm máu; những xét nghiệm này cũng giúp phân biệt nó với bệnh nhược cơ (myasthenia gravis), một bệnh thần kinh cơ tự miễn có ảnh hưởng tới dẫn truyền thần kinh-cơ.[4]
Nếu hội chứng nhược cơ Lambert–Eaton có liên quan đến ung thư, điều trị trực tiếp khối ung thư thường làm thuyên giảm các triệu chứng. Các phương pháp điều trị khác thường được sử dụng là steroid, azathioprine, có tác dụng ức chế hệ miễn dịch, globulin miễn dịch truyền tĩnh mạch (IVIg), hoạt động bằng cách cạnh tranh với tự kháng thể tại thụ thể Fc; pyridostigmine và 3,4-diaminopyridine, các thuốc này có tác dụng tăng cường dẫn truyền thần kinh-cơ. Trao đổi huyết tương (PLEX) đôi khi được chỉ định để loại bỏ kháng thể khỏi hệ tuần hoàn.[4]
Tình trạng này ảnh hưởng đến khoảng 3,4 trên một triệu người.[1] Hội chứng nhược cơ Lambert–Eaton thường xảy ra ở người trên 40 tuổi, nhưng có thể gặp ở bất kỳ độ tuổi nào.
Triệu chứng cơ năng và triệu chứng thực thể Hội chứng nhược cơ Lambert–Eaton
Yếu cơ trong hội chứng Lambert–Eaton chủ yếu ảnh hưởng đến các cơ gốc chi ở tay và chân (những cơ gần thân mình). Khác với bệnh nhược cơ (myasthenia gravis), tình trạng yếu cơ thường ảnh hưởng chân nhiều hơn tay, gây khó khăn khi leo cầu thang và đứng dậy từ tư thế ngồi. Cơ lực có thể cải thiện tạm thời sau khi gắng sức hoặc tập thể dục. Nhiệt độ cơ thể cao có thể làm triệu chứng nặng thêm. Yếu cơ hành tủy (các cơ vùng miệng và họng) đôi khi xảy ra.[4] Yếu cơ vận nhãn ít gặp. Một số trường hợp có thể bị nhìn đôi, sụp mí mắt và khó nuốt,[4] nhưng nhìn chung chỉ xuất hiện kèm theo yếu chân. Đặc điểm này giúp phân biệt Hội chứng Lambert-Eaton với bệnh nhược cơ. Trong bệnh nhược cơ các dấu hiệu ở mắt hay gặp hơn nhiều.[3] Ở giai đoạn tiến triển của bệnh, có thể xuất hiện yếu cơ hô hấp.[4] Một số người cũng có thể gặp vấn đề về phối hợp vận động (thất điều).[5]
Có đến ba phần tư số người mắc hội chứng Lambert–Eaton gặp rối loạn chức năng của hệ thần kinh tự chủ. Biểu hiện có thể bao gồm khô miệng, táo bón, nhìn mờ, giảm tiết mồ hôi và hạ huyết áp tư thế đứng (huyết áp giảm khi đứng dậy, có thể dẫn đến ngất xỉu). Một số người cảm thấy vị kim loại trong miệng.[4]
Bên cạnh việc khai thác bệnh sử và khám lâm sàng bởi bác sĩ chuyên khoa thần kinh-cơ, xét nghiệm tìm kháng thể kháng kênh calci đóng mở bằng điện áp (VGCC) và điện cơ (EMG) có thể giúp chẩn đoán hội chứng nhược cơ Lambert–Eaton. Tuy nhiên, kết quả dương tính với kháng thể VGCC cũng có thể gặp ở bệnh lý khác. Sức cơ cải thiện hơn khi kiểm tra lặp lại nhiều lần, ví dụ lực bóp tay tăng lên khi bóp liên tục (một hiện tượng được gọi là “dấu hiệu Lambert”). Ở trạng thái nghỉ ngơi, các phản xạ thường giảm; nhưng sau khi vận động cơ, đáp ứng phản xạ lại tăng lên. Đây là một đặc điểm điển hình của hội chứng Lambert–Eaton. Phản xạ ánh sáng đồng tử có thể chậm hơn bình thường.[4]
Trong hội chứng Lambert–Eaton liên quan ung thư phổi tế bào nhỏ, đa số bệnh nhân không có triệu chứng gợi ý ung thư tại thời điểm chẩn đoán, chẳng hạn như ho, ho ra máu và sụt cân. Tuy nhiên, các triệu chứng Lambert–Eaton có thể xuất hiện đến 5 năm trước khi chẩn đoán ung thư, hoặc cũng có thể xuất hiện sau khi đã chẩn đoán ung thư.[3] Hội chứng Lambert–Eaton có liên quan ung thư phổi thường nặng hơn hội chứng không do ung thư gây ra.[5]
Nguyên nhân Hội chứng nhược cơ Lambert–Eaton
Hội chứng Lambert–Eaton thường liên quan đến ung thư phổi (50–70% trường hợp), đặc biệt là ung thư tế bào nhỏ,[4] khiến hội chứng này được xếp vào nhóm hội chứng cận u.[5] Trong số những người mắc ung thư phổi tế bào nhỏ, 1–3% đồng thời mắc hội chứng Lambert–Eaton.[3] Trong đa số trường hợp đó, hội chứng Lambert–Eaton là triệu chứng đầu tiên của ung thư phổi, và ngoài ra bệnh nhân không có triệu chứng gì khác của ung thư.[3]
Hội chứng Lambert–Eaton cũng có liên quan đến bệnh nội tiết, chẳng hạn như suy giáp hoặc đái tháo đường type 1.[4][6] Bệnh nhược cơ cũng có thể xảy ra khi có khối u (u tuyến ức). Người mắc nhược cơ không kèm u, và người mắc hội chứng Lambert–Eaton không kèm u, đều có các biến thể di truyền tương tự nhau làm tăng nguy cơ mắc các bệnh này.[3] Đặc biệt, yếu tố HLA-DR3-B8 (một phân nhóm của hệ thống kháng nguyên bạch cầu người HLA) dường như làm tăng nguy cơ mắc hội chứng Lambert–Eaton.[6]
Cơ chế Hội chứng nhược cơ Lambert–Eaton
Sinh lý bình thường
Trong hoạt động thần kinh-cơ bình thường, xung thần kinh được truyền dọc theo sợi trục thần kinh từ tủy sống xuống đến đầu tận cùng của dây thần kinh tại khớp nối thần kinh-cơ, nơi xung động thần kinh được truyền sang tế bào cơ. Đến đầu tận cùng thần kinh ở synap, luồng xung thần kinh này làm mở các kênh calci đóng mở bằng điện áp (VGCC), cho phép ion calci tràn vào đầu mút dây thần kinh, và sự gia tăng nồng độ calci sẽ kích hoạt các bóng synap hòa vào màng tế bào để giải phóng chất dẫn truyền thần kinh. Các túi synap này chứa acetylcholin, và khi hòa màng chúng phóng thích acetylcholin vào khe synap, acetylcholin gắn vào các thụ thể acetylcholin ở phía tế bào cơ, khiến cơ co lại.[4]
Bệnh lý của hội chứng Lambert–Eaton
Trong hội chứng Lambert–Eaton, cơ thể sinh ra các kháng thể chống lại kênh calci loại VGCC, đặc biệt là kênh calci loại P/Q (và có thể cả loại N), làm giảm lượng ion calci có thể đi vào đầu mút dây thần kinh, hậu quả là giảm lượng acetylcholin được giải phóng vào synap thần kinh-cơ. Ngoài cơ vân, hệ thần kinh tự chủ cũng cần acetylcholin để dẫn truyền tín hiệu; điều này giải thích tại sao hội chứng Lambert–Eaton lại gây ra các triệu chứng rối loạn tự chủ.[4][3] Kênh calci P/Q còn hiện diện ở tiểu não, giải thích vì sao một số bệnh nhân bị thất điều.[5][6] Các kháng thể tập trung gắn với phần của thụ thể được gọi là "peptide liên kết miền III S5–S6" (domain III S5–S6 linker peptide).[6] Kháng thể cũng có thể liên kết với các kênh calci phụ thuốc điện thế khác khác.[6] Một số có kháng thể liên kết với synaptotagmin, loại protein cảm ứng calci điều hòa việc các túi synap hợp màng để phóng thích chất dẫn truyền thần kinh.[6] Nhiều bệnh nhân Lambert–Eaton, bao gồm cả những người không có kháng thể chống VGCC, lại có kháng thể kháng thụ thể acetylcholin loại M1. Sự hiện diện của các kháng thể này có thể góp phần lý giải vì sao dòng calci vào tế bào thần kinh bị giảm đến mức cơ thể mất bù.[6]
Ngoài việc giảm dòng calci đi vào, còn xảy ra sự gián đoạn tại các vị trí phóng thích túi synap trong vùng hoạt động (active zone). Có thể cũng do kháng thể gây ra, vì người mắc hội chứng Lambert–Eaton có kháng thể chống lại một số thành phần của các vùng hoạt động này (bao gồm các kênh calci phụ thuộc điện áp). Những bất thường kể trên dẫn đến sự giảm khả năng co cơ. Nếu kích thích lặp đi lặp lại liên tục trong khoảng 10 giây, cuối cùng một lượng calci đủ lớn sẽ vào được đầu mút thần kinh, và sức co của cơ tăng lên đến gần mức bình thường. Hiện tượng này có thể quan sát được khi thực hiện điện cơ kim: tăng biên độ CMAP (điện thế hoạt động cơ toàn phần) xảy ra khi kích thích lặp lại kéo dài.[4]
Trong hội chứng Lambert–Eaton đi kèm ung thư phổi, các kháng thể gây bệnh cũng gắn vào kênh calci trên tế bào ung thư; người ta cho rằng các kháng thể này ban đầu phát triển như một phản ứng của hệ miễn dịch đối với tế bào ung thư.[4] Có giả thuyết cho rằng rằng phản ứng miễn dịch chống lại tế bào ung thư đã kìm hãm sự phát triển của khối u, nhờ đó tiên lượng ung thư cải thiện hơn.[3][6]
Chẩn đoán Hội chứng nhược cơ Lambert–Eaton

Chẩn đoán thường được thực hiện bằng phương pháp đo dẫn truyền thần kinh (NCS) và điện cơ (EMG), một trong những xét nghiệm tiêu chuẩn trong việc điều tra tình trạng yếu cơ không rõ nguyên nhân. Điện cơ là phương pháp dùng kim nhỏ châm vào cơ để ghi lại hoạt động điện của cơ, còn nghiên cứu dẫn truyền thần kinh được thực hiện bằng cách kích thích các dây thần kinh bằng những xung điện nhẹ trên bề mặt da và đo đáp ứng điện học của cơ tương ứng. Trong hội chứng Lambert–Eaton, thăm dò NCS tập trung đánh giá điện thế hoạt động cơ toàn phần (CMAP) ở các cơ bị ảnh hưởng; đôi khi kỹ thuật điện cơ sợi đơn (single-fiber EMG) cũng được sử dụng.[4]
Khi đo điện dẫn truyền với kích thích lặp lại tần số 2 lần/giây (2 Hz), bình thường biên độ CMAP sẽ giảm dần do acetylcholin ở đầu nối thần kinh-cơ bị cạn kiệt. Ở hội chứng Lambert–Eaton, mức giảm biên độ này lớn hơn so với bình thường. Sau đó, khi acetylcholin dự trữ được huy động bổ sung, biên độ CMAP sẽ tăng trở lại. Tuy nhiên, trong hội chứng Lambert–Eaton, sự tăng này vẫn không đủ để đạt ngưỡng truyền đạt xung động từ dây thần kinh sang cơ, do đầu tận cùng thần kinh không tiếp nhận đủ lượng calci. (Một kiểu mẫu tương tự cũng được quan sát thấy ở bệnh nhược cơ). Ngược lại, khi cho người bệnh vận động cơ trước, biên độ CMAP ở bệnh nhân Lambert–Eaton tăng lên rất nhiều (trên 200%, thậm chí nhiều hơn). Hiện tượng tương tự cũng xảy ra nếu áp một chuỗi kích thích điện nhanh (20 xung mỗi giây trong 10 giây). Điều này là do dòng ion calci tràn vào đầu mút thần kinh nhằm đáp ứng các kích thích trên.[3][4] Ở thăm dò điện cơ sợi đơn, các dấu hiệu có thể bao gồm độ giao động thời gian (jitter) giữa các xung động tăng lên (cũng thấy trong các bệnh rối loạn truyền tin thần kinh-cơ khác) và hiện tượng block dẫn truyền.[4]
Các xét nghiệm máu có thể được tiến hành để loại trừ những nguyên nhân khác gây bệnh lý cơ: ví dụ, creatin kinase (CK) tăng cao có thể gợi ý viêm cơ, và xét nghiệm chức năng tuyến giáp bất thường có thể gợi ý bệnh cơ do nhiễm độc giáp (cường giáp). Kháng thể kháng kênh calci đóng mở điện áp (VGCC) có thể tìm thấy ở 85% người bệnh hội chứng Lambert–Eaton được chẩn đoán bằng điện cơ. Sau khi chẩn đoán xác định hội chứng Lambert–Eaton, các thăm dò như chụp cắt lớp vi tính lồng ngực thường được tiến hành để tìm khối u phổi tiềm ẩn. Khoảng 50–60% số khối u được phát hiện ngay sau khi chẩn đoán hội chứng Lambert–Eaton; số còn lại được chẩn đoán muộn hơn, nhưng thường trong vòng hai năm (điển hình là trong bốn năm) kể từ khi chẩn đoán hội chứng Lambert–Eaton.[3] Do đó, việc thực hiện chẩn đoán hình ảnh được khuyến cáo lặp lại mỗi sáu tháng trong hai năm đầu sau chẩn đoán.[4] Mặc dù chụp cắt lớp vi tính (CT) phổi thường đủ để tầm soát, phương pháp chụp cắt lớp phát xạ positron toàn thân (chụp PET) cũng có thể được thực hiện nhằm tìm các khối u tiềm ẩn, đặc biệt ở phổi.[7]
Điều trị Hội chứng nhược cơ Lambert–Eaton

Nếu hội chứng nhược cơ Lambert–Eaton do một loại ung thư tiềm ẩn gây ra, điều trị khối ung thư đó có thể giúp các triệu chứng của hội chứng thuyên giảm hoặc biến mất.[4] Việc điều trị thường bao gồm hóa trị, với xạ trị ở những người mắc bệnh ở giai đoạn ung thư khu trú.[3]
Thuốc Firdapse hiện là phương pháp duy nhất được Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) chấp thuận để điều trị hội chứng Lambert–Eaton. Firdapse tác động lên phần trước synap của thần kinh-cơ, làm tăng giải phóng acetylcholin, từ đó giúp cải thiện chức năng cơ và giảm nhẹ các triệu chứng của hội chứng này.[8]
Ức chế miễn dịch
Một số bằng chứng ủng hộ hiệu quả của globulin miễn dịch truyền tĩnh mạch (IVIg) trong điều trị.[9] Tuy nhiên, việc ức chế miễn dịch nói chung có xu hướng kém hiệu quả hơn so với ở các bệnh tự miễn khác. Prednisolon (một glucocorticoid, tức steroid) có tác dụng ức chế đáp ứng miễn dịch, và azathioprine có thể được dùng thay thế sau khi prednisolon đã đạt hiệu quả điều trị mong muốn. IVIG cũng có thể được kết hợp sử dụng và cho một mức độ hiệu quả nhất định. Trao đổi huyết tương (hoặc lọc huyết tương, PLEX), loại bỏ các protein huyết tương như kháng thể và thay thế bằng huyết tương bình thường, có thể cải thiện tình trạng nhược cơ cấp, đe dọa tính mạng. Tuy nhiên, trao đổi huyết tương ở hội chứng nhược cơ Lambert–Eaton kém hiệu quả hơn so với trong các bệnh liên quan (như bệnh nhược cơ), và thường cần dùng thêm các thuốc ức chế miễn dịch khác hỗ trợ.[4]
Khác
Ba phương pháp điều trị khác cũng nhằm mục đích cải thiện triệu chứng của hội chứng Lambert–Eaton, đó là pyridostigmine, 3,4-diaminopyridine (còn gọi là amifampridine) và guanidine. Các thuốc này đều giúp tăng cường dẫn truyền thần kinh-cơ. Ngoài ra, IVIg và thuốc Mestinon (pyridostigmine dạng uống) được xem là các điều trị hỗ trợ thứ yếu cho hội chứng này.[10]
Một số bằng chứng ở quy mô nhỏ cho thấy 3,4-diaminopyridine có hiệu quả ít nhất trong vài tuần đầu điều trị.[9] Có thể sử dụng 3,4-diaminopyridine ở dạng base hoặc dạng muối phosphat tan trong nước.[11] Cả hai dạng thuốc này đều làm chậm quá trình tái phân cực tại đầu mút dây thần kinh sau khi phát xung, nhờ đó cho phép nhiều ion calci tích lũy hơn trong đầu tận của dây thần kinh.[4][3]
Pyridostigmine làm giảm sự phân hủy acetylcholin sau khi giải phóng vào khe synap, nhờ đó cải thiện sự co cơ. Một thuốc cũ hơn là guanidine gây nhiều tác dụng phụ và không được khuyến cáo sử dụng. 4-aminopyridine (dalfampridine), một thuốc liên quan đến 3,4-diaminopyridine, cũng gây tác dụng phụ nhiều hơn 3,4-DAP và không được khuyến cáo dùng.[3]
FDA đã phê duyệt amifampridine để sử dụng cho trẻ em từ 6 tuổi trở lên mắc hội chứng Lambert–Eaton (bổ sung vào phê duyệt trước đó cho người lớn) vào ngày 28 tháng 11 năm 2018.[8]
Lịch sử Hội chứng nhược cơ Lambert–Eaton
Anderson và cộng sự từ Bệnh viện St Thomas, London, là những người đầu tiên đề cập đến một trường hợp có thể có các biểu hiện lâm sàng của hội chứng Lambert–Eaton vào năm 1953.[12] Tuy nhiên, phải đến năm 1956, các bác sĩ Edward H. Lambert, Lee Eaton và E.D. Rooke tại Bệnh viện Mayo mới là những người đầu tiên mô tả đầy đủ các phát hiện lâm sàng và điện sinh lý của bệnh này.[13] Năm 1972, việc ghi nhận hội chứng Lambert–Eaton thường xuất hiện cùng các bệnh tự miễn khác đã dẫn đến giả thuyết cho rằng hội chứng này do cơ chế tự miễn gây ra.[14] Các nghiên cứu vào những năm 1980 đã xác nhận bản chất tự miễn,[6] và nghiên cứu vào những năm 1990 đã chứng minh mối liên hệ giữa hội chứng Lambert–Eaton với sự hiện diện của kháng thể chống lại kênh calci đóng mở điện áp loại P/Q.[4][15]
Tham khảo Hội chứng nhược cơ Lambert–Eaton
- 1 2 Titulaer, Maarten J.; Lang, Bethan; Verschuuren, Jan Jgm (tháng 12 năm 2011). "Lambert-Eaton myasthenic syndrome: from clinical characteristics to therapeutic strategies" [Hội chứng nhược cơ Lambert-Eaton: từ đặc điểm lâm sàng đến chiến lược điều trị]. The Lancet. Neurology (bằng tiếng Anh). Quyển 10 số 12. tr. 1098–1107. doi:10.1016/S1474-4422(11)70245-9. ISSN 1474-4465. PMID 22094130.
- ↑ "Myasthenic syndrome - Definition, Meaning & Synonyms" [Hội chứng nhược cơ - Định nghĩa, ý nghĩa và từ đồng nghĩa]. Vocabulary.com (bằng tiếng Anh). Truy cập ngày 21 tháng 2 năm 2026.
- 1 2 3 4 5 6 7 8 9 10 11 12 13 Verschuuren, Jan J. G. M.; Wirtz, Paul W.; Titulaer, Maarten J.; Willems, Luuk N. A.; van Gerven, Joop (tháng 7 năm 2006). "Available treatment options for the management of Lambert-Eaton myasthenic syndrome" [Các phương pháp điều trị hội chứng nhược cơ Lambert-Eaton hiện nay]. Expert Opinion on Pharmacotherapy (bằng tiếng Anh). Quyển 7 số 10. tr. 1323–1336. doi:10.1517/14656566.7.10.1323. ISSN 1744-7666. PMID 16805718.
- 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 Mareska, Michael; Gutmann, Laurie (tháng 6 năm 2004). "Lambert-Eaton myasthenic syndrome" [Hội chứng nhược cơ Lambert-Eaton]. Seminars in Neurology (bằng tiếng Anh). Quyển 24 số 2. tr. 149–153. doi:10.1055/s-2004-830900. ISSN 0271-8235. PMID 15257511.
- 1 2 3 4 Rees, J. H. (tháng 6 năm 2004). "Paraneoplastic syndromes: when to suspect, how to confirm, and how to manage" [Hội chứng cận u: khi nào nghi ngờ, làm thế nào để xác định và phương hướng điều trị]. Journal of Neurology, Neurosurgery, and Psychiatry (bằng tiếng Anh). Quyển 75 Suppl 2 số Suppl 2. tr. ii43–50. doi:10.1136/jnnp.2004.040378. ISSN 0022-3050. PMC 1765657. PMID 15146039.
- 1 2 3 4 5 6 7 8 9 Takamori, Masaharu (ngày 15 tháng 9 năm 2008). "Lambert-Eaton myasthenic syndrome: search for alternative autoimmune targets and possible compensatory mechanisms based on presynaptic calcium homeostasis" [Hội chứng nhược cơ Lambert-Eaton: Tìm kiếm các mục tiêu tự miễn thay thế và các cơ chế bù trừ khả thi dựa trên cân bằng nội môi của calci tiền synap.]. Journal of Neuroimmunology (bằng tiếng Anh). Quyển 201–202. tr. 145–152. doi:10.1016/j.jneuroim.2008.04.040. ISSN 0165-5728. PMID 18653248.
- ↑ Ropper AH, Brown RH (2005). "53. Myasthenia Gravis and Related Disorders of the Neuromuscular Junction" [Bệnh nhược cơ và các rối loạn liên quan đến khớp nối thần kinh cơ]. Trong Ropper AH, Brown RH (biên tập). Adams and Victor's Principles of Neurology (bằng tiếng Anh) (ấn bản thứ 8). New York: McGraw-Hill Professional. tr. 1261. ISBN 0-07-141620-X.
- 1 2 "Firdapse FDA Approval History" [Lịch sử phê duyệt của FDA đối với Firdapse]. Drugs.com (bằng tiếng Anh). ngày 25 tháng 6 năm 2024. Truy cập ngày 21 tháng 2 năm 2026.
- 1 2 Keogh, Michael; Sedehizadeh, Saam; Maddison, Paul (ngày 16 tháng 2 năm 2011). "Treatment for Lambert-Eaton myasthenic syndrome" [Điều trị hội chứng nhược cơ Lambert-Eaton]. The Cochrane Database of Systematic Reviews (bằng tiếng Anh). Quyển 2011 số 2. tr. CD003279. doi:10.1002/14651858.CD003279.pub3. ISSN 1469-493X. PMC 7003613. PMID 21328260.
- ↑ Illa, Isabel (tháng 5 năm 2005). "IVIg in myasthenia gravis, Lambert Eaton myasthenic syndrome and inflammatory myopathies: current status" [Thực trạng điều trị bằng IVIg trong bệnh nhược cơ, hội chứng nhược cơ Lambert Eaton và các bệnh viêm cơ]. Journal of Neurology (bằng tiếng Anh). Quyển 252 Suppl 1. tr. I14–18. doi:10.1007/s00415-005-1104-5. ISSN 0340-5354. PMID 15959667.
- ↑ Stangel, Martin; Lindquist (tháng 5 năm 2011). "Update on treatment options for Lambert–Eaton myasthenic syndrome: focus on use of amifampridine" [Cập nhật về các lựa chọn điều trị hội chứng nhược cơ Lambert-Eaton: tập trung vào việc sử dụng amifampridine]. Neuropsychiatric Disease and Treatment (bằng tiếng Anh). tr. 341. doi:10.2147/NDT.S10464. ISSN 1176-6328. PMC 3148925. PMID 21822385.
- ↑ Anderson, H (tháng 12 năm 1953). "Bronchial neoplasm with myasthenia; prolonged apnea after administration of succinylcholine" [U phế quản kèm theo nhược cơ; ngưng thở kéo dài sau khi dùng succinylcholine]. The Lancet (bằng tiếng Anh). Quyển 262 số 6799. tr. 1291–1293. doi:10.1016/S0140-6736(53)91358-0. Truy cập ngày 21 tháng 2 năm 2026.
- ↑ Lambert EH, Eaton LM, Rooke ED (1956). "Defect of neuromuscular conduction associated with malignant neoplasms" [Rối loạn dẫn truyền thần kinh cơ liên quan đến u ác tính]. Am. J. Physiol. (bằng tiếng Anh). Quyển 187. tr. 612–613.
- ↑ Gutmann, L.; Crosby, T. W.; Takamori, M.; Martin, J. D. (tháng 9 năm 1972). "The Eaton-Lambert syndrome and autoimmune disorders" [Hội chứng Eaton-Lambert và các rối loạn tự miễn]. The American Journal of Medicine (bằng tiếng Anh). Quyển 53 số 3. tr. 354–356. doi:10.1016/0002-9343(72)90179-9. ISSN 0002-9343. PMID 4115499.
- ↑ Motomura, M.; Hamasaki, S.; Nakane, S.; Fukuda, T.; Nakao, Y. K. (tháng 8 năm 2000). "Apheresis treatment in Lambert-Eaton myasthenic syndrome" [Điều trị bằng phương pháp lọc huyết tương trong hội chứng nhược cơ Lambert-Eaton]. Therapeutic Apheresis: Official Journal of the International Society for Apheresis and the Japanese Society for Apheresis (bằng tiếng Anh). Quyển 4 số 4. tr. 287–290. doi:10.1046/j.1526-0968.2000.004004287.x. ISSN 1091-6660. PMID 10975475.
Liên kết ngoài Hội chứng nhược cơ Lambert–Eaton
- Bệnh tự miễn
- Bệnh thần kinh cơ và khớp nối thần kinh cơ
- Hội chứng cận u

