Số phối trí
Trong hóa học, tinh thể học và khoa học vật liệu, số phối trí của một nguyên tử trung tâm trong một phân tử hay một tinh thể là số nguyên tử, phân tử hay ion liên kết với nguyên tử trung tâm đó. Các ion/phân tử/nguyên tử bao quanh ion/phân tử/nguyên tử trung tâm được gọi là phối tử. Cách xác định giá trị này sẽ thay đổi tùy theo dạng phức chất là tinh thể hay phân tử.
Đối với các phân tử và ion đa nguyên tử, số phối trí của một nguyên tử được xác định bằng cách đếm các nguyên tử khác mà nó liên kết (bằng liên kết đơn hoặc liên kết đa).[1] Ví dụ, phức chất [Cr(NH3)2Cl2Br2]− có Cr3+ là cation trung tâm và có số phối trí là 6. Các số phối trí thường thấy là 4, 6 và 8.
Phân tử, ion đa nguyên tử và phức chất

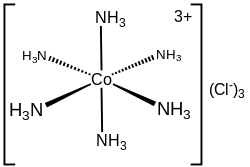

Trong hóa học, số phối trí, được Alfred Werner định nghĩa lần đầu tiên vào năm 1893, là các nguyên tử lân cận của một nguyên tử trung tâm trong một phân tử hoặc ion.[1][3] Khái niệm này được áp dụng phổ biến nhất trong phức chất.
Các trường hợp đơn giản và phổ biến
Số phối trí phổ biến nhất cho kim loại chuyển tiếp khối d là 6. Số phối trí không phân biệt hình học của các phức chất, chẳng hạn như giữa lăng trụ bát diện và lăng trụ tam giác.
Đối với các kim loại chuyển tiếp, số phối trí dao động từ 2 (ví dụ là AuI trong Ph3PAuCl) đến 9 (ví dụ là ReVII trong [ReH9]2−). Kim loại khối f (họ lanthan và actini) có thể có số phối trí cao hơn nhờ có bán kính ion lớn hơn và nhiều orbital để tạo liên kết hơn.
Số phối trí từ 8 đến 12 thường được thấy ở các nguyên tố khối f. Ví dụ, khi có các ion nitrat hai càng làm phối tử, thì CeIV và ThIV sẽ có số phối trí là 12 và từ đó sẽ có các phức chất [Ce(NO3)6]2− và [Th(NO3)6]2−. Khi các phối tử xung quanh nhỏ hơn đáng kể so với nguyên tử trung tâm, thì có thể tạo ra các phức chất có số phối trí cao. Một bài nghiên cứu dùng hóa học tính toán đã dự đoán được ion PbHe2+
15 ổn định trong đó có một ion chì phối trí với ít nhất 15 nguyên tử heli.[4] Trong số các pha Frank–Kasper, việc xếp chặt các nguyên tố kim loại có thể cho số phối trí lên đến 16.[5] Ở chiều ngược lại, án ngữ không gian có thể cho ra các số phối trí đặc biệt thấp. Một trường hợp mà kim loại có số phối trí là 1 cực kỳ hiếm gặp là trong phức hợp arylthallium(I) gốc terphenyl 2,6-Tipp2C6H3Tl, trong đó Tipp là nhóm 2,4,6-triisopropylphenyl.[6]
Phối tử polyhapto
Số phối trí trở nên phức tạp hơn khi đề cập đến các phối tử polyhapto. Đối với các phối tử có electron π như ion cyclopentaidienide [C5H5]−, các alken và ion cyclooctatetraenide [C8H8]2−, số nguyên tử liền kề hệ thộng electron mà liên kết tới nguyên tử trung tâm được gọi là hapticity. Trong ferrocene, độ hapto, η, của mỗi anion cyclopentadienide là năm, từ đó có công thức Fe(η5-C5H5)2. Có nhiều cách để xác định mức độ đóng góp vào số phối trí của nguyên tử sắt trung tâm từ mỗi phối tử cyclopentadienide. Đóng góp này có thể được tính là một vì chỉ có một phối tử, hoặc là năm vì có năm nguyên tử liền kề, hoặc là ba vì có ba cặp electron tham gia liên kết. Thông thường, người ta đếm cặp electron để xác định việc này.[7]
Trong mạng tinh thể
Số phối trí có thể được xác định rõ ràng đối với các nguyên tử bên trong mạng tinh thể bằng cách đếm các lân cận gần nhất theo mọi hướng. Số lượng lân cận của một nguyên tử bên trong được gọi là số phối trí khối (bulk coordination number). Đối với các bề mặt, vì số nguyên tử lân cận bị hạn chế hơn, nên số phối trí bề mặt (surface coordination number) sẽ nhỏ hơn số phối trí khối. Thông thường, số phối trí bề mặt không xác định hoặc có thể tùy biến.[8] Số phối trí bề mặt cũng phụ thuộc vào chỉ số Miller của bề mặt. Trong tinh thể lập phương tâm khối (BCC), số phối trí khối là 8, trong khi đó, đối với bề mặt (100), số phối trí bề mặt là 4.[9]
Xác định bằng thực nghiệm
Một cách phổ biến để xác định số phối trí của một nguyên tử là tinh thể học tia X. Các phương pháp liên quan gồm có tán xạ neutron hoặc electron.[10] Số phối trí của một nguyên tử có thể xác định dễ dàng bằng cách đếm các ion/phân tử/nguyên tử cận kề.
Ví dụ, α-Nhôm có cấu trúc lập phương tâm mặt, trong đó mỗi nguyên tử nhôm có 12 nguyên tử cận kề, 6 nguyên tử trong cùng mặt phẳng, và 3 nguyên tử nằm trên và nằm dưới và đa diện phối trí là một khối lập phương. α-Sắt có cấu trúc lập phương tâm khối trong đó mỗi nguyên tử sắt có 8 nguyên tử kề cận ở các góc của khối lập phương.

Hai thù hình phổ biến nhất của carbon có số phối trí khác nhau. Trong kim cương, mỗi nguyên tử carbon nằm ở tâm của một tứ diện đều được tạo thành bởi bốn nguyên tử carbon khác, số phối trí trong trường hợp này là 4, tương tự như trong methan. Than chì được cấu tạo từ các lớp hai chiều, trong đó mỗi nguyên tử carbon liên kết cộng hóa trị với ba nguyên tử carbon khác; các nguyên tử ở các lớp khác nằm xa hơn và không phải là nguyên tử lân cận gần nhất, từ đó số phối trí là 3.[11]


Đối với các hợp chất có mạng tinh thể đều đặn như natri chloride hay caesi chloride thì có thể hình dung được môi trường xung quanh ion bằng cách đếm các ion lân cận. Trong natri chloride, mỗi ion natri có 6 ion chloride lân cận (cách 276 pm) ở các góc của khối bát diện và mỗi ion chloride có 6 nguyên tử natri (cũng cách 276 pm) tại các góc của một khối bát diện. Trong caesi chloride, mỗi caesi có 8 ion clorua bao quanh (cách 356 pm) ở các góc của một khối lập phương và mỗi clorua có 8 ion caesi (cũng cách 356 pm) tại các góc của một khối lập phương.
Bất cập
Liên đoàn Tinh thể học Quốc tế, IUCr, quy định rằng số phối trí của một nguyên tử trong chất rắn kết tinh phụ thuộc vào mô hình liên kết hóa học và cách tính số phối trí.[12][13]
Trong một số kim loại, khoảng cách giữa liên kết kim loại-phối tử có thể thay đổi. Một ví dụ là trong PbCl2, số phối trí của Pb2+ sẽ phụ thuộc vào việc chloride nào sẽ được coi là phối tử. 7 phối tử chloride cho độ dài liên kết Pb-Cl là 280–309 pm. Hai phối tử chloride còn lại thì cách xa hơn, với độ dài liên kết Pb-Cl là 370 pm.[14]
Một số kim loại có cấu trúc bất thường, chẳng hạn như kẽm với cấu trúc lục giác xếp chặt méo mó. Trong cấu trúc lục giác xếp chặt, mỗi nguyên tử sẽ cận kề với 12 nguyên tử khác và một cấu hình triangular orthobicupola.[15][16] Trong kẽm có 6 nguyên tử gần nhất với khoảng cách 266 pm từ trung tâm trong cùng một mặt phẳng đóng gói chặt chẽ với 6 nguyên tử gần nhất tiếp theo, cách đều nhau, ba nguyên tử lân cận trong mỗi mặt phẳng xếp chặt ở trên và dưới với khoảng cách 291 pm. Vì vậy mà số phối trí của kẽm có thể là 12 thay vì là 6.[13] Có thể áp dụng cách thức này cho cấu trúc khối lập phương tâm khối đều đặn, trong đó ngoài 8 nguyên tử lân cận nhất còn có thêm 6 nguyên tử láng giềng nữa, cách xa hơn khoảng 15%,[15] và trong trường hợp này, số phối trí thường được coi là 14.

Trong Nickel arsenide (NiAs) và vài hợp chất liên quan, số phối trí của kim loại không thể xác định rõ ràng. Kim loại trung tâm tạo liên kết với sáu phối tử As, nhưng cũng có thể coi hai tiếp điểm Ni---Ni là một liên kết.[15]
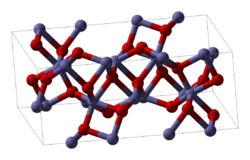
Hai ví dụ khác về các hóa chất thường gặp là Fe2O3 và TiO2. Fe2O3 ó cấu trúc tinh thể có thể được mô tả là có một mảng gần như đóng gói chặt chẽ các nguyên tử oxy với các nguyên tử sắt lấp đầy hai phần ba các lỗ bát diện. Tuy nhiên, mỗi nguyên tử sắt có 3 nguyên tử lân cận gần nhất và 3 nguyên tử khác ở xa hơn một chút. Cấu trúc khá phức tạp: các nguyên tử oxy được phối hợp với bốn nguyên tử sắt và các nguyên tử sắt lần lượt chia sẻ các đỉnh, cạnh và mặt của bát diện bị biến dạng.[15] TiO2 có cấu trúc rutil. Các nguyên tử titan có số phối trí là 6, trong đó 2 nguyên tử cách 198,3 pm và 4 nguyên tử cách 194,6 pm trong cấu trúc bát diện hơi bị biến dạng. Các bát diện xung quanh các nguyên tử titan chia sẻ các cạnh và đỉnh để tạo thành một mạng lưới 3 chiều. Các ion oxide có số phối trí là 3 trong cấu hình phẳng tam giác.[17]
Tham khảo
- 1 2 IUPAC, Compendium of Chemical Terminology (Giản lược thuật ngữ hoá học), bản thứ 2 ("Gold Book") (1997). Bản đã chỉnh sửa trực tuyến: (2006–) "coordination number". doi:10.1351/goldbook.C01331
- ↑ Haaland, Arne; Shorokhov, Dmitry J.; Tutukin, Andrey V.; Volden, Hans Vidar; Swang, Ole; McGrady, G. Sean; Kaltsoyannis, Nikolas; Downs, Anthony J.; Tang, Christina Y.; Turner, John F. C. (2002). "Molecular Structures of Two Metal Tetrakis(tetrahydroborates), Zr(BH4)4 and U(BH4)4: Equilibrium Conformations and Barriers to Internal Rotation of the Triply Bridging BH4 Groups". Inorganic Chemistry. 41 (25): 6646–6655. doi:10.1021/ic020357z. PMID 12470059.
- ↑ De, A.K. (2003). A Text Book of Inorganic Chemistry. New Age International Publishers. tr. 88. ISBN 978-8122413847.
- ↑ Hermann, Andreas; Lein, Matthias; Schwerdtfeger, Peter (2007). "The Search for the Species with the Highest Coordination Number". Angewandte Chemie International Edition. 46 (14): 2444–7. doi:10.1002/anie.200604148. PMID 17315141.
- ↑ Sinha, Ashok K. (1972). "Topologically close-packed structures of transition metal alloys". Progress in Materials Science. 15 (2). Elsevier BV: 81–185. doi:10.1016/0079-6425(72)90002-3. ISSN 0079-6425.
- ↑ Niemeyer, Mark; Power, Philip P. (ngày 18 tháng 5 năm 1998). "Synthesis and Solid-State Structure of 2,6-Trip2C6H3Tl (Trip=2,4,6-iPr3C6H2): A Monomeric Arylthallium(I) Compound with a Singly Coordinated Thallium Atom". Angewandte Chemie International Edition (bằng tiếng Anh). 37 (9): 1277–1279. doi:10.1002/(SICI)1521-3773(19980518)37:9<1277::AID-ANIE1277>3.0.CO;2-1. ISSN 1521-3773. PMID 29711226.
- ↑ Crabtree, Robert H. (2009). The Organometallic Chemistry of the Transition Metals. John Wiley & Sons. ISBN 9780470257623.
- ↑ De Graef, Marc; McHenry, Michael E. (2007). Structure of Materials: An Introduction to Crystallography, Diffraction and Symmetry (PDF). Cambridge University Press. tr. 515. ISBN 978-0-521-65151-6. Bản gốc (PDF) lưu trữ ngày 29 tháng 4 năm 2021. Truy cập ngày 15 tháng 3 năm 2019.
- ↑ "Closest Packed Structures". Chemistry LibreTexts. ngày 2 tháng 10 năm 2013. Truy cập ngày 28 tháng 7 năm 2020.
- ↑ Massa, Werner (1999). Crystal Structure Determination . Springer. tr. 67–92.
- ↑ Wells, A.F. (1984). Structural Inorganic Chemistry (ấn bản thứ 5). Oxford Science Publications. ISBN 978-0198553700.
- ↑ "II. Coordination of the atoms". Bản gốc lưu trữ ngày 13 tháng 6 năm 2012. Truy cập ngày 9 tháng 11 năm 2014.
- 1 2 Mittemeijer, Eric J. (2010). Fundamentals of Materials Science: The Microstructure–Property Relationship using metals as model systems. Springer. ISBN 9783642105005.
- ↑ Wells A. F. (1984) Structural Inorganic Chemistry 5th edition Oxford Science Publications ISBN 0-19-855370-6
- 1 2 3 4 Wells, A.F. (1984). Structural Inorganic Chemistry (ấn bản thứ 5). Oxford Science Publications. ISBN 978-0198553700.
- ↑ Piróth, A.; Sólyom, Jenö (2007). Fundamentals of the Physics of Solids: Volume 1: Structure and Dynamics. Springer. tr. 227. ISBN 9783540726005.
- ↑ Diebold, Ulrike (2003). "The surface science of titanium dioxide". Surface Science Reports. 48 (5–8): 53–229. Bibcode:2003SurSR..48...53D. doi:10.1016/S0167-5729(02)00100-0. ISSN 0167-5729.
